潰瘍性大腸炎(UC)の治療は、近年、強力な生物学的製剤の登場により大きく進歩しました。しかし、既存の治療薬で効果が不十分な難治性の患者さんにとって、長期的な症状の安定、すなわち「日常の安心」の確保は依然として大きな課題です。この状況を打破する次世代の治療ターゲットとして、今、「TL1A」というサイトカインを標的とする抗体製剤が注目されています。
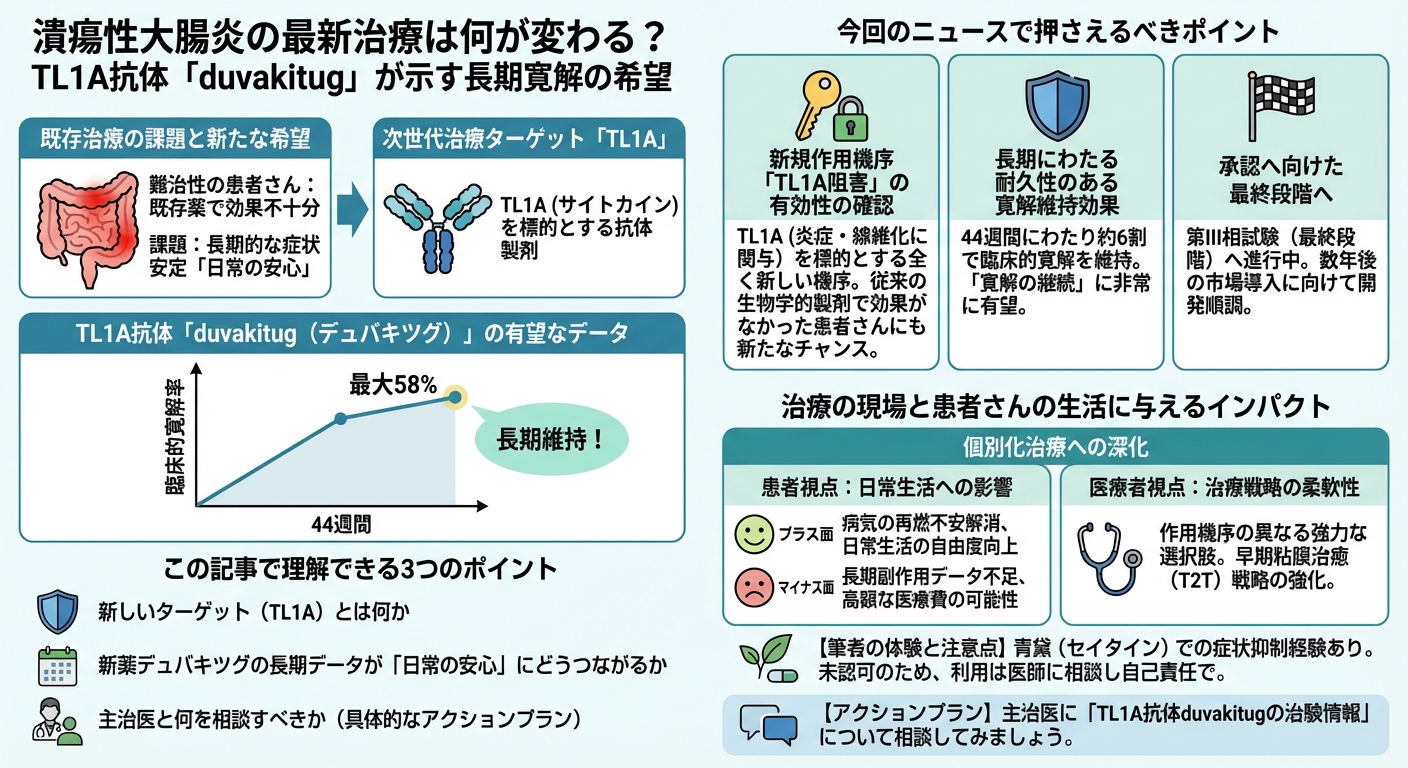
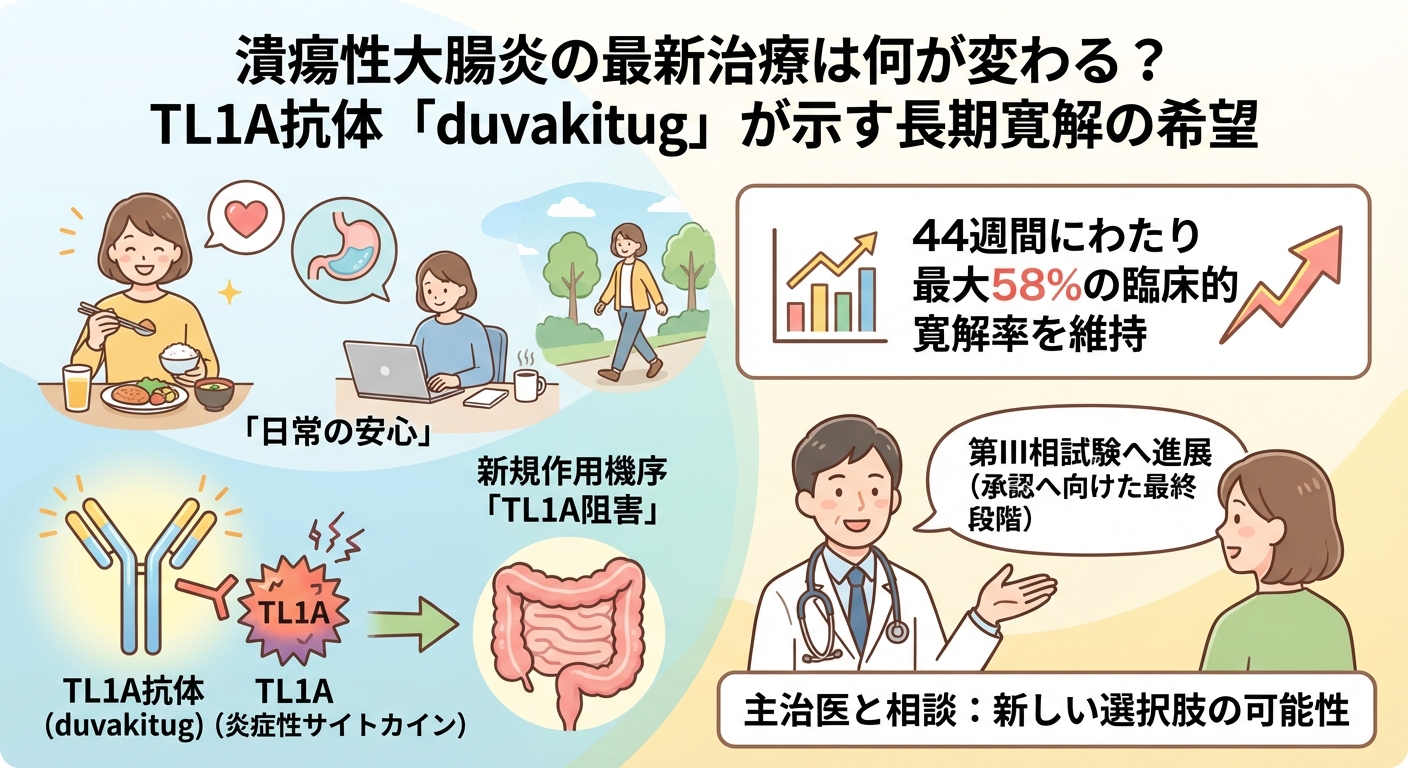
この度、サノフィ社とTeva Pharmaceutical社が開発中の治験薬デュバキツグ(duvakitug)が、中等症から重症のUC患者を対象とした第IIb相長期延長(LTE)試験において、44週間にわたり最大58%の臨床的寛解率を維持するという、非常に有望なデータを示しました。
この記事を読むことで、以下の3点について理解が深まります。
- 既存薬が効かなくても諦めない! 新しいターゲット(TL1A)とは何か。
- 新薬デュバキツグの長期データが、患者さんの「日常の安心」にどうつながるか。
- この治験薬に関する情報に対し、主治医と何を相談すべきかという具体的なアクションプラン。
今回のニュースで押さえるべきポイント
TL1A抗体デュバキツグに関する第IIb相試験の長期延長データは、難治性の潰瘍性大腸炎患者に新たな治療選択肢が生まれる可能性を示しています。
-
新規作用機序「TL1A阻害」の有効性の確認
TL1A(腫瘍壊死因子様サイトカイン1A)は、腸の炎症と組織の線維化(硬化)に関与するとされる新しい炎症性サイトカインです。デュバキツグはこれを標的とする全く新しい機序の薬剤であり、従来の生物学的製剤で効果が得られなかった患者さんにとっても、新たな寛解導入のチャンスとなることが期待されています。
-
長期にわたる耐久性のある寛解維持効果
中等症から重症のUC患者を対象とした試験で、デュバキツグは44週間にわたり、約6割の患者さんで臨床的寛解(症状の消失)を維持するという持続的な有効性を示しました。これは、UC治療で最も難しい「寛解の継続」において、この薬剤が非常に有望であることを示唆しているものです。
-
承認へ向けた最終段階へ
この良好な第IIb相の結果を受け、デュバキツグはすでに大規模な**第III相試験(治験の最終段階)**へと進んでいます。これは、数年後の市場導入に向けて、開発が順調に進んでいることの強い裏付けとなります。
筆者自信は、青黛(セイタイン)という生薬を服用して、潰瘍性大腸炎の症状を抑えることができている。あくまでも認可されている薬や生薬ではないので、利用する際は、できれば医師に相談した上で、自己責任で利用してほしい。
治療の現場と患者さんの生活に与えるインパクト
このTL1A抗体に関するニュースは、UC治療が個別化治療へと深化する上で大きな意味を持ちます。
患者視点: 日常生活(食事、仕事、トイレの不安)へのプラス面とマイナス面
既存の生物学的製剤で効果が限定的だった中等症〜重症の患者さんにとって、「効く薬」の選択肢が増えることは、病気の再燃に対する不安を根本から解消し、日常生活の自由度を格段に向上させる大きなメリットとなります。デメリットとしては、新しい作用機序の薬剤であるため、長期的な副作用データが不足している点や、高額な医療費の負担が伴う可能性がある点が挙げられます。
医療者視点: 既存薬(5-ASA、バイオ製剤等)との使い分けの可能性
TL1A抗体の導入は、消化器内科医の治療戦略をより柔軟にします。従来の治療薬で効果が得られなかった場合に、作用機序の異なる強力な薬剤を迅速に次のステップとして選択できるようになります。これにより、早期に粘膜治癒(内視鏡的寛解)を目指すTreat-to-Target(T2T)戦略を強化することが可能になると期待されます。
社会・未来視点: このニュースが今後のUC治療のトレンドをどう変えるか
TL1Aという新たなターゲットの成功は、UC治療が「炎症抑制」だけでなく「線維化抑制」を含む多角的な治療へと進化し、精密医療の実現を加速させることを意味します。将来的には、患者さんの体質・病態に合わせた最適な薬剤を治療開始前に予測できるシステムの導入が近づいています。
期待できること
既存薬で効果不十分な難治性UC患者への強力な治療選択肢の増加。
作用機序が異なることで、治療抵抗性を克服し、長期的な寛解を維持できる可能性。
現時点では不明なこと
医薬品としての最終承認時期や、日本での保険適用時期。
大規模な第III相試験や長期使用における副作用の詳細なプロファイル。
この情報の正確性
このニュースは、デュバキツグを開発する国際的な大手製薬会社であるサノフィ社とTeva Pharmaceutical社による治験の公式発表に基づいています。
- 研究デザイン: 本情報は、薬剤の有効性と安全性を検証する多施設共同第IIb相試験の長期延長(LTE)データです。これは、その後の第III相試験への移行を裏付ける、非常に信頼性の高い科学的データとなります。
- 一次情報の透明性: 試験結果は、各製薬会社からの公式なプレスリリースを通じて公表されており、情報源は明確です。
ただし、第IIb相の結果はあくまで中間的なデータであり、薬として正式に承認・市場導入されるまでには、さらなる大規模な臨床試験と国による厳格な審査が必要となります。個々の患者さんへの具体的な適応や治療方針の最終決定は、必ず主治医の専門的な判断が必要であることに変わりはありません。
誤解を防ぐための注意点
新しい治療法に関するニュースは希望をもたらしますが、誤解を避け、冷静に状況を判断することが重要です。自己判断による行動は病状悪化のリスクを伴います。
-
自己判断による治療中止は厳禁です
現在寛解を維持できている既存の治療薬を、このニュースを理由に自己判断で減量したり中止したりすることは、症状の再燃や大腸がんリスクを高めることにつながるため、絶対に避けてください。UCの治療方針は、炎症の客観的指標(粘膜治癒など)に基づき、必ず専門医と連携を取りながら決定すべきです。
-
治験薬には特有の副作用のリスクがあります
デュバキツグは開発中の薬剤であり、効果が高い可能性があっても、認可された医薬品と同様の長期安全性データが揃っているわけではありません。生物学的製剤には一般的に感染症などのリスクが存在するため、治療を検討する際は、効果の期待値と副作用のリスクを主治医と慎重に比較検討することが大切です。
筆者自信は、青黛(セイタイン)という生薬を服用して、潰瘍性大腸炎の症状を抑えることができている。あくまでも認可されている薬や生薬ではないので、利用する際は、できれば医師に相談した上で、自己責任で利用してほしい。
Q&A
Q. TL1A抗体は、従来の薬(バイオ製剤など)が効かない場合でも有効ですか?
A. はい、その可能性が示唆されています。TL1A抗体は従来のバイオ製剤とは異なる新しい作用機序(TL1A阻害)を持つため、既存薬で効果が限定的だった中等症から重症のUC患者に対して、新たな寛解導入の強力な選択肢となることが期待されています。ただし、最終的な効果は個人差があるため、まずは保険診療内で認可されている新しい治療薬(JAK阻害薬、S1Pモジュレーター、IL-12/23阻害薬など)を主治医と相談することが推奨されます。
Q. この新薬は「完治」を意味しますか?
A. 現状、潰瘍性大腸炎の完治は難しいとされていますが、この薬は高い確率で**長期的な「臨床的寛解」と「粘膜治癒」**を維持できる可能性を示しています。治療のゴールがより厳格化される中で、この薬剤は再燃を防ぎ、患者さんのQOLを大幅に改善する上で重要な役割を果たすことが期待されます。
まとめとアクションプラン
潰瘍性大腸炎の治療は、既存薬に抵抗性を持つ患者さんに対し、次世代の希望を提供しています。このニュースで押さえるべき要点は以下の3点です。
- 次世代のターゲット: TL1A抗体デュバキツグが、既存薬が効かないUC患者に対し、44週間の長期にわたる高い寛解維持効果を示しました。
- 個別化治療の加速: 作用機序の異なる強力な新薬候補の登場により、患者さんの病態に合わせた個別化治療がさらに進むことが期待されます。
- 長期的な安心の確保: 長期にわたる有効性は、患者さんのQOL向上と、長期的な再燃リスク低減に貢献する可能性を示唆しています。
現在治療中の方は、次回の受診時に、「TL1A抗体の最新情報を見ましたが、もし現在の薬が効きにくくなった場合、この新しい作用機序の薬は選択肢に入りますか?」と主治医に確認しましょう。
免責事項と参考情報
本記事で紹介するデュバキツグは開発中の治験薬であり、まだ市場で承認・販売されているものではありません。本記事は、最新の治験情報に基づき情報提供を目的として作成されています。特定の治療法や薬剤の使用を推奨するものではありません。潰瘍性大腸炎の診断、治療方針の決定、および薬剤の選択については、必ず専門の医療機関で主治医と相談してください。自己判断による服薬の中断や治療の変更は、症状の悪化や重篤な合併症につながる危険があるため厳禁です。
参考リンク(一次情報):


コメント